業績推移
| 業績の推移(百万円) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| 売上高 | 営業利益 | % | 経常利益 | % | 当期利益 | % | 一株利益 | 一株配当 | |
財務
| 財務・CF(百万円) 2020/09/30 | |||
|---|---|---|---|
| 総資産 | 5,249 | 営業CF | -632 |
| 純資産 | 4,806 | 投資CF | 86 |
| 自己資本比率 | 0.9 % | 財務CF | 2,786 |
| 資本金 | 8,849 | 現金等 | 3,643 |
四半期推移表
| 四半期 | 1Q | 2Q | 3Q | 4Q | ||||
|---|---|---|---|---|---|---|---|---|
| 前期 | 今期 | 前期 | 今期 | 前期 | 今期 | 前期 | 今期 | |
| 累計 | 1Q | 1-2Q | 1-3Q | 1-4Q | 会社予想 | ||||
|---|---|---|---|---|---|---|---|---|---|
| 前期 | 今期 | 前期 | 今期 | 前期 | 今期 | 前期 | 今期 | 今期 | |
リンクボタン
トピックス
リスク・対策
2【事業等のリスク】
有価証券報告書に記載した事業の状況、経理の状況等に関する事項のうち、経営者が提出会社の財政状態、経営成績及びキャッシュ・フローの状況に重要な影響を与える可能性があると認識している主要なリスクは、以下のとおりであります。また、当社は必ずしも事業上のリスクとは考えていない事項についても、投資家の投資判断上、重要であると考えられる事項については、投資家に対する情報開示の観点から積極的に開示しております。
なお、当社は、これらのリスク発生の可能性を認識した上で、発生の回避及び発生した場合の対応等に努める方針でありますが、投資判断は、以下の記載事項及び本項以外の記載事項を慎重に検討した上で行われる必要があります。以下の記載は、当社に関連するリスクを全て網羅するものではないことにご留意ください。
なお、文中の将来に関する事項は、当有価証券報告書提出日現在において当社が判断したものであります。
①価格に係るリスク
免疫細胞治療は先進的な医療技術であるため、一般的な治療として行われている外科療法、放射線療法、化学療法(抗がん剤治療等)等のように、現時点では保険診療の対象とはなっておらず、当社契約医療機関における免疫細胞治療1クールの治療費総額は、医師が適切と判断する治療の種類等にもよりますが、およそ160万円であります。当社は、特定細胞加工物の製造の対価として細胞加工の種類と回数に基づく変動課金制による加工料を頂いておりますが、その金額は当該契約医療機関の患者が負担する治療費に制約されます。また、免疫細胞治療は先端医療であるがゆえに、医師の治療方法に対する考え方に相違があること、関連技術が急速な進歩過程にあること等の理由により、標準的な価格水準が定まっていません。今後、免疫細胞治療の治療費水準の変化等に伴い、加工料の見直しがなされた場合には、当社の業績に影響を与える可能性があります。また、2014年11月に「再生医療等安全性確保法」が施行され、免疫細胞治療は医療機関により適切に提供されることになりましたが、今後、本法令を遵守した運用の中で新たな対応策が求められる可能性も考えられることから、特定細胞加工物の製造の対価そのものの形態が変更される可能性があります。
企業が細胞加工を受託する「細胞加工業」というビジネスモデル構築の過程において、どのような価格体系が形成されるかは今後の動向次第であり、そのため免疫細胞治療に係る価格については未だ不確定要素があります。
今後、再生・細胞医療分野の産業化に向けた環境が整備され、多くの新規企業による市場参入及び競争激化に伴い、特定細胞加工物の製造の対価及び新たなビジネスの価格競争が生じた場合には、当社業績に影響を与える可能性があります。
②競合及び競合他社に係るリスク
(1)再生・細胞医療に係る分野への企業参入状況
「再生医療関連法」の施行は、これまで明確な法的枠組みが整わなかったために再生・細胞医療市場への参入を控えていた製薬企業等が参入する機会となり得ます。現在、複数の企業が、当社のビジネスと類似したモデルで免疫細胞治療を含む再生・細胞医療に係る分野に参入してきております。こうした動きは、新たな技術革新の進展を促し、市場が拡大していく反面、玉石混淆の状況を作り出す可能性もあり、結果として患者のデメリットになることも考えられます。他企業がトラブルを起こした場合、業界全体のイメージ低下等により、当社も間接的に悪影響を受け、当社の業績に影響を与える可能性があります。
(2)バイオテクノロジーの進歩に伴う競合
当社の属するバイオテクノロジー業界は急速に変化・拡大しておりますが、特にがん治療分野では新しい治療薬の研究開発が進んでおります。大手製薬企業が、がんをターゲットとして開発を進める免疫チェックポイント阻害薬(がんの免疫逃避機構を阻止する薬)、分子標的薬(病気に関係がある細胞だけに働きかける機能を持った新しいタイプの治療薬)、血管新生阻害剤(がん細胞に栄養や酸素を供給する血管の新生を抑える薬)等は免疫細胞治療との併用効果が期待されておりますが、仮に免疫細胞治療との併用とは関連なく、治療効果の高い医薬品が開発された場合には、当社の業績に影響を与える可能性があります。
また、当社においては、積極的な研究開発投資により、常に最先端の技術への対応、業界に先駆けた新技術の開発等に注力しておりますが、当該技術革新への対応が遅れた場合、あるいは、現在の主力事業の対象となっている免疫細胞治療に代わる画期的な治療法が開発された場合等には、当社の業績に影響を与える可能性があります。
③品質管理体制に係るリスク
当社は、2014年に施行された再生医療関連法の下、これまで培った経験・知見、再生・細胞医療分野の事業ノウハウを用いて効率的に適合させ、信頼ある細胞加工業を推進しております。現在、当社では以下のような品質管理体制を整備・運用しております。
(1)細胞培養加工施設
当社が細胞加工を行っている品川細胞培養加工施設は、「再生医療等安全性確保法」に適合する設備構造を有しており、2015年5月に特定細胞加工物製造事業者許可を取得し、医療機関、企業等からの細胞加工を受託できる体制が整っております。
(2)細胞加工技術者の育成・確保
「再生医療等安全性確保法」の施行により、企業が医療機関から治療用細胞の加工を受託することが可能となっております。十分な安全管理体制を確保できない医療機関や細胞培養加工施設を有しながらも効率的な運営ができない等の問題を抱える医療機関から治療用細胞の加工を受託することが可能となり、当社にとってこれまでの事業経験をアドバンテージとして、営業収益を拡大する機会となります。しかしながら、治療用細胞を適正かつ安全に加工するためには、十分な教育を受けた細胞加工技術者の確保・育成が必須です。当社ではこれまでの経験に裏付けされた治療用細胞の加工を適正かつ安全に行うための細胞加工技術者の育成システムを有しており、継続的に細胞加工技術者を育成・確保に努めております。
(3)原材料管理
細胞加工には常に安全な原材料を用いることが条件となるため、培地(細胞培養液)や試薬については、購入先との厳密な購買契約を締結し、培地や試薬の不良品の混入、劣化を未然に防ぐとともに、仕入、保存管理の徹底、検査体制の充実等、常に品質管理体制の強化を図っております。
当社は、今後とも常に品質管理体制の強化に努めてまいりますが、人材流出、培地や試薬の不良品の混入、劣化、細胞加工の過程における人為的な過失、地震や火災の災害等が発生した場合には、重大な事故に繋がる恐れもあり、当社の業績に影響を与える可能性があります。また、再生医療関連法が施行された下で運営されている細胞培養加工施設の前例がまだ少なく、新たに定められた法律であるため、関係官庁の動向や当社が想定し得ない事象が生じた場合には、その対応の為、当社の事業推進に影響を与える可能性があります。
④法的規制の影響
当社は、事業の遂行にあたって、関連法令を含めた法令を遵守しております。主には、次に挙げる再生医療関連法の法的規制の適用を受けています。
(1)「再生医療等安全性確保法」との関連
「再生医療等安全性確保法」は、再生医療等に用いられる再生医療等技術の安全性の確保及び生命倫理への配慮や医療機関が再生医療技術を用いた治療を行う場合に講じるべき措置、治療に用いる細胞組織の加工を医療機関以外が実施する場合の細胞加工物の製造の許可等の制度を定めた法律です。今後、治療に用いる細胞加工を行う場合には、細胞培養加工施設ごとに「特定細胞加工物製造業許可」を取得する必要があります(但し、医療機関が細胞加工を行う場合には届出のみ)。医療機関が再生医療を行おうとする場合には、再生医療等提供計画の作成、認定再生医療等委員会における審議、厚生労働省への計画書等の提出が義務付けられます。そのため、医療機関にとっては、こうした手続き等の負担が大きくなりますが、一方で、こうした適切な治療手続きを行っていない医療機関等は排除されていくことになります。
当社は、上記のような医療機関に対して法律対応を支援するとともに、特定細胞加工物製造事業者許可を取得した当社が保有する細胞培養加工施設で医療機関からの細胞加工を受託しております。しかしながら、新たに定められた法律であるため、関係官庁の動向や当社が想定し得ない事象が生じた場合には、その対応のためのコストが発生する可能性があり、そのため、当社の財政状態に影響を及ぼす可能性があります。
(2)「医薬品医療機器等法」との関連
「医薬品医療機器等法」は、医薬品、医薬部外品、化粧品及び医療機器の品質、有効性及び安全性の確保のために必要な規制を行うとともに、指定薬物の規制に関する措置を講ずるほか、医療上特にその必要性が高い医薬品及び医療機器の研究開発の促進のために必要な措置、医薬品等の有効性及び安全性の確保のために必要な規制を行うことを目的とした法律です。本法律では、再生医療技術を用いた医療用の製品として、新たに再生医療等製品がカテゴリ化されており、当社が再生医療技術を用いた医療用の製品開発を行う場合には、当法律に従うことになります。
再生医療関連法には罰則が規定されており、「再生医療等安全性確保法」に関しては当社及び契約医療機関が、「医薬品医療機器等法」に関しては当社及び当社が技術導入・導出した企業等が、予期せず当該罰則規定に抵触した場合には、罰則金の支払いが生じること等から、当社の社会的な信用を失う可能性があります。
⑤研究開発に内在する不確実性
当社が事業展開する再生・細胞医療分野は、日進月歩に進化するがゆえに、継続的な研究開発活動は持続的成長にとって大変重要な役割を担っております。
当社では、研究開発を通して将来に渡る企業価値向上を図るべく、研究開発を戦略的に遂行していくための体制を構築し、積極的な活動を行っております。
これらに必要な研究開発費は、2018年9月期1,502,882千円(売上高に対する比率150.5%)、2019年9月期276,566千円(同比率26.1%)、2020年9月期249,996千円(同比率31.9%)となっており、将来に渡る企業価値向上を図るための先行投資と認識しております。
しかしながら、研究開発投資に見合うだけの事業化等による研究成果が得られなかった場合等には、当社の業績に影響を与える可能性があります。
⑥知的財産権に係るリスク
医療技術や細胞加工に密接に関わる重要な(周辺)技術については、積極的に知的財産権の出願を行い、当社の技術を適切に保護しております。
また、これら先端医療技術の中には、特許として知的財産権を獲得するよりも、ノウハウとして保有する方が事業戦略上優位であると考えられるものも少なからずあり、ノウハウについては、取引先あるいは共同研究先との秘密保持契約等で守ることにより、外部に流出しないよう厳しく管理しております。
しかしながら、以上のような対応している中においても、出願した案件が権利化できないという可能性もあり、また、権利化できた場合でも、実際にその権利を行使できない可能性や、第三者の権利に抵触している可能性もあります。
⑦政府の推進政策等の変化
現在、日本においては、再生医療関連法の施行等により、再生・細胞医療分野に関する規制制度環境が整備されております。また、それ以外にも再生・細胞医療、バイオテクノロジー及び先端医療に係る各種の推進政策が実施されており、これらの推進政策は、当社が事業を展開する細胞加工事業及び再生医療等製品事業等の分野に大きく関わっております。
政府の主な推進政策とその概要は以下のとおりであります。
(1)新たな成長戦略テーマとしての医療関連産業
日本経済の再生に向けた成長戦略の一環として2016年2月に閣議決定された「日本再興戦略-第4次産業革命に向けて-」の官民戦略プロジェクト10において、医療関連産業の活性化を行うための方策として、医薬品・医療機器開発・再生医療研究を加速させる規制・制度改革等が含まれる等、近年、成長産業としての医療分野の注目度が急速に高まってきております。上記戦略においては、医療などの社会保障関連分野が有望成長市場の一つに位置づけられ、「世界最先端の健康立国へ」として日本発の優れた医薬品・医療機器等の開発・事業化、グローバル市場の獲得・国際貢献を行うこと等が盛り込まれていることから、その政策動向如何により、当社の今後の事業展開に影響を与えるものと考えております。
(2)先進医療制度
日本における医療制度においては、保険診療と保険で認められていない診療(保険外診療)の併用は原則として禁止されております。しかし、将来的に保険導入を目指す先端的医療技術については、「先進医療」という制度によって保険診療との併用が認められています。これにより今後、「先進医療」として免疫細胞治療を実施する医療機関が増え、免疫細胞治療の認知、普及がさらに進むことが期待されます。しかしながら、今後、これら政府の政策の方向性に大きな変化が生じることとなった場合には、当社の業績に影響を与える可能性があります。
⑧特定の取引先への依存
2020年9月期の売上高783,035千円のうち、医療法人社団滉志会に対する売上は、604,904千円(売上高に占める割合77.3%)と、現時点では同医療法人に対する依存度が高い状態にあります。医療法人社団滉志会は、当社と緊密かつ安定的な関係にありますが、今後両者の関係が悪化した場合や、万が一同医療法人において不慮の事故が発生すること等により受診患者数の減少、閉鎖等の事態に至った場合には、当社の業績に影響を与える可能性があります。
⑨再生医療等製品事業に係るリスク
当社は、計画的に再生医療等製品の開発を進め、最終的には再生医療等製品の製造販売承認を取得することにより、再生医療等製品事業を細胞加工業に続く新たな収益の柱とすることを目指してまいります。再生医療等製品開発においては、計画の進捗管理のためにマイルストーンを設け、マイルストーンごとに検証を加えながら慎重に再生医療等製品開発を進めてまいりますが、再生医療等製品の臨床試験において必ずしも当社の期待したとおりの結果が得られるとは限らず、結果として再生医療等製品の製造販売承認が得られなかった場合には、当社の業績に影響を与える可能性があります。
⑩マイナスの利益剰余金
当社は、多額の研究開発費用が先行して計上されること等により、2011年9月期より10期連続して当期純損失を計上しており、当事業年度末では利益剰余金の欠損額7,352,457千円を計上するに至っております。来期以降もこれまで事業の中核をなしていた契約医療機関向けの特定細胞加工物の製造に加えて、企業等に向けた細胞加工業への展開等、新たなビジネス領域を拡大することで、早期の黒字化を目指してまいります。さらに、再生医療等製品の開発を加速させ、製造販売承認を取得することで、収益化することにより、利益剰余金の欠損額の解消を目指してまいります。しかしながら、当社の売上高が計画通りに確保できず、今後も当期純利益を獲得出来ない場合、利益剰余金のマイナスが長期に渡って継続する可能性があります。
⑪資金調達に関する事項
当社は、当事業年度において第16回及び第17回新株予約権の発行による資金調達を実施したこともあり、当事業年度末の手元資金(現金及び預金)残高は3,643,814千円となり財政基盤は安定しております。しかしながら当事業年度においては営業活動によるキャッシュ・フローがマイナスであり、今後の当社の財政状態、経営成績及びキャッシュ・フローの状況、また金融市場の状況等によっては、資金調達が困難になる可能性があります。その場合には、再生医療等製品の開発や細胞培養加工施設等への設備投資等が計画通りに進められず、当社の事業の推進に影響が及ぶ可能性があります。
⑫継続企業の前提に関する重要事象等
当社は、がん免疫療法市場の環境変化に伴う細胞加工業の売上急減に加え、再生医療等製品事業分野における自社製品の開発進捗に伴う支出が累増しているため、継続的に営業損失及びマイナスの営業キャッシュ・フローが発生しており、継続企業の前提に疑義を生じさせるリスクが存在しております。
しかしながら、当社は、2018年4月に開始した事業構造改革を着実に実行することで、細胞加工業セグメントにおいては、細胞加工施設の統廃合、希望退職募集の実施等を通じて製造体制の適正化を図り、同セグメントのセグメント利益の早期黒字化を目指しております。また、再生医療等製品事業セグメントにおいては、早期の製造販売承認の取得に向けて有望でかつ可能性の高いシーズを優先して開発を進めるとともに、再生医療等製品の開発費等については資金状況を勘案の上、機動的に資金調達を実施してまいります。現状では、構造改革の着実な実行を通じた資金の確保、さらに2019年6月の第14回及び第15回、2020年7月の第16回並びに2020年9月の第17回新株予約権の発行による再生医療等製品開発費の資金調達等により、安定的なキャッシュポジションを維持しており、当面の資金繰りに懸念はないものと判断しております。これらに加えて、当社における当事業年度末の資金残高の状況を総合的に検討した結果、事業活動の継続性に疑念はなく、継続企業の前提に関する重要な不確実性は認められないものと判断しております。
⑬新型コロナウイルス感染症の影響
新型コロナウイルス感染症の世界的な拡大については、未だに収束の見通しが立っておらず、引き続き企業活動や経済活動への制限を余儀なくされるような厳しい状況が続くものと想定されます。当社においては、取引先医療機関でのインバウンドの患者数の減少による細胞加工売上の減少や一部取引先の資金繰りの悪化による貸倒懸念債権の発生等の影響が生じております。現時点において、新型コロナウイルス感染症の収束時期や企業活動、経済活動の回復時期を見通すことは困難であり、今後、新型コロナウイルス感染症の拡大により、当社の従業員や取引先でクラスター(集団感染)が発生した場合、品川細胞培養加工施設の操業の中断・遅延などにより、当社の業績及び財政状態に影響を及ぼす可能性があります。
当社は、新型コロナウイルス感染症の対策として、品川細胞培養加工施設での細胞加工体制維持のため、細胞加工技術者を対象とした健康管理(検温、手洗い、消毒)の実施を、同施設に立ち入る全ての従業員、来客に対象を拡大するとともに、細胞加工技術者以外の職員の在宅勤務推進、社外来訪者並びに本社職員の同施設への立入制限等を行うことにより、職員の感染の防止に努めております。
経営指標の推移
(1)連結経営指標等
回次 | 第21期 | 第22期 | 第23期 | 第24期 | 第25期 | |
決算年月 | 2016年9月 | 2017年9月 | 2018年9月 | 2019年9月 | 2020年9月 | |
売上高 | (千円) | 1,909,324 | 1,704,004 | 998,278 | - | - |
経常損失(△) | (千円) | △1,823,818 | △1,745,839 | △2,711,641 | - | - |
親会社株主に帰属する当期純損失(△) | (千円) | △1,643,198 | △2,603,685 | △3,048,545 | - | - |
包括利益 | (千円) | △1,681,603 | △2,381,992 | △3,339,938 | - | - |
純資産額 | (千円) | 5,931,081 | 5,480,081 | 3,313,101 | - | - |
総資産額 | (千円) | 7,646,578 | 6,265,673 | 3,937,155 | - | - |
1株当たり純資産額 | (円) | 63.51 | 50.28 | 27.56 | - | - |
1株当たり当期純損失(△) | (円) | △18.01 | △27.24 | △26.77 | - | - |
潜在株式調整後1株当たり当期純利益 | (円) | - | - | - | - | - |
自己資本比率 | (%) | 77.0 | 86.9 | 82.8 | - | - |
自己資本利益率 | (%) | △25.2 | △46.0 | △70.0 | - | - |
株価収益率 | (倍) | - | - | - | - | - |
営業活動によるキャッシュ・フロー | (千円) | △1,088,096 | △1,333,145 | △2,499,487 | - | - |
投資活動によるキャッシュ・フロー | (千円) | 430,269 | 199,714 | 154,386 | - | - |
財務活動によるキャッシュ・フロー | (千円) | 440,297 | 975,814 | 1,110,214 | - | - |
現金及び現金同等物の期末残高 | (千円) | 3,594,270 | 3,436,654 | 2,201,767 | - | - |
従業員数 | (人) | 170 | 156 | 92 | - | - |
(外、平均臨時雇用者数) | (32) | (37) | (30) | (-) | (-) | |
(注)1.売上高には、消費税等は含まれておりません。
2.潜在株式調整後1株当たり当期純利益については、潜在株式は存在するものの1株当たり当期純損失であるため記載しておりません。
3.株価収益率については、親会社株主に帰属する当期純損失であるため記載しておりません。
4.従業員数には、契約医療機関への出向者を含めております。
5.第24期より連結財務諸表を作成しておりませんので、第24期及び第25期の連結経営指標等は記載しておりません。
事業内容 / ビジネスモデル
3【事業の内容】
当社は、「常に本質を究め、誠実性と公正性をもって真の社会的付加価値を創造する」という経営理念の下、「次世代の医療を支える革新的な技術及びサービスを迅速かつ効率的に社会に提供し続ける」ことにより、人々の健康と“quality of life(生活の質)”の向上に資することを使命として、細胞加工業及び再生医療等製品事業を展開しております。
当社の当事業年度末における事業内容は次のとおりであります。
なお、次の2部門は「第5 経理の状況 1 財務諸表等 (1)財務諸表 注記事項(セグメント情報等)」に掲げるセグメントの区分と同一であります。
① 細胞加工業
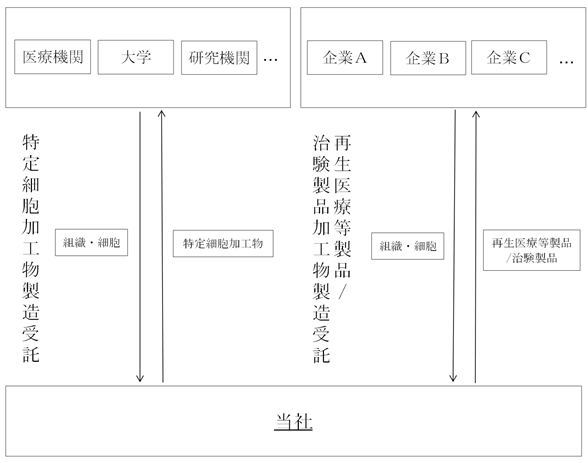
細胞加工業では、企業、大学、医療機関/研究機関等から、臨床用の細胞加工及び治験用の細胞加工物製造の受託、再生・細胞医療のバリューチェーン事業、細胞培養加工施設の運営管理、細胞加工技術者の派遣・教育システムの提供等を行っております。
ⅰ)細胞加工業について
細胞加工業のビジネスモデルを図示すると、以下のとおりであります。
(参考)2020年9月30日現在の主な当社契約医療機関
名称 | 住所 |
医療法人社団 滉志会 |
|
瀬田クリニック東京 | 東京都千代田区神田駿河台2-1-45ニュー駿河台ビル3階 |
国立病院機構大阪医療センター | 大阪府大阪市中央区法円坂2-1-14 |
医療法人社団葵会aoi国際病院 | 神奈川県川崎市川崎区田町2-9-1 |
一般社団法人健康医学協会粒子線がん相談クリニック | 東京都千代田区紀尾井町4-1 |
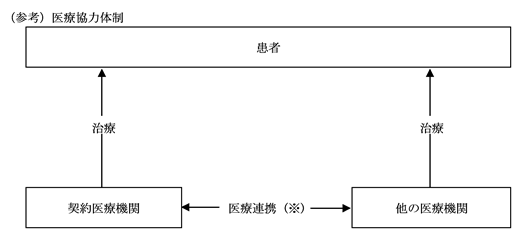
※ 免疫細胞治療を希望する患者の多くは、既に他の医療機関で一般的な治療を受けており、契約医療機関を受診する際には、これまでの病歴等、診療上十分な医療情報を共有することが必要となることから、医療機関同士が連携して医療が行われております。また、免疫細胞治療を希望する患者のうち、医療上の理由等で、契約医療機関を受診できない患者については、患者の要請に基づき、他の医療機関で治療を実施される場合があります。この場合、他の医療機関と契約医療機関では、医療連携として十分な医療情報の交換がなされ、共同で治療が実施されます。
ⅱ)バリューチェーン事業について
バリューチェーン事業を図示すると、以下のとおりであります。
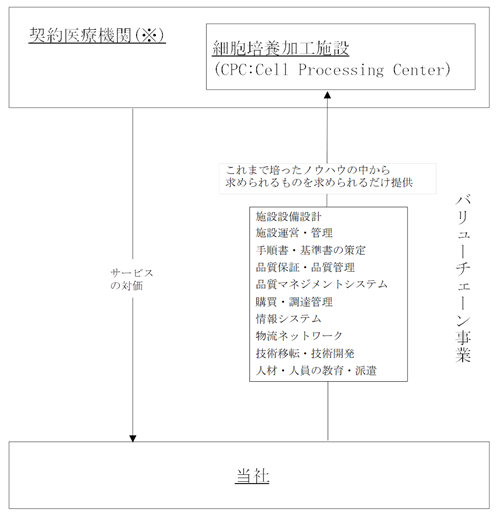
※ 契約医療機関は、当社の細胞医療技術に限らず、独自の再生・細胞医療技術に係る臨床研究等を行っております。
(参考)2020年9月30日現在の当社契約医療機関
名称 | 住所 |
国立大学法人金沢大学 | 石川県金沢市角間町ヌ7 |
学校法人順天堂 順天堂大学 | 東京都文京区本郷2-1-1 |
当社は、このようなサービスを医療機関に提供することにより、再生・細胞医療の普及発展、難治性疾患の治療に貢献するとともに、事業の拡大を図ってまいります。
② 再生医療等製品事業
再生医療等製品事業では、当社で行う研究開発のみならず、これまで継続的に行ってきた大学病院等との共同研究を通じて、再生医療等製品の製造販売承認を取得してまいります。同時に、国内外で行われている再生医療等製品の開発動向にも注目し、国内外の有望な技術・物資等を持つ企業等とのアライアンスにより、パイプラインの拡充を視野に入れた活動も行っております。
再生医療等製品事業について
再生医療等製品事業のビジネスモデルを図示すると、以下のとおりであります。
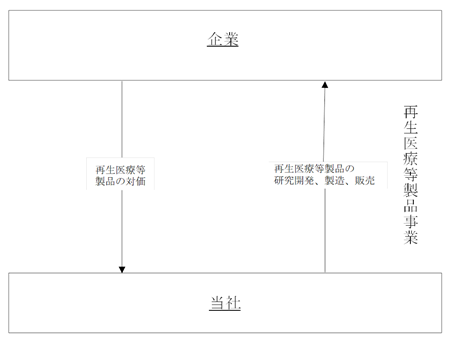
再生医療等製品事業においては、再生医療等製品の製造・販売承認を取得し、上市・販売するための研究開発を行っております。
決算(通期)
当事業年度(2019年10月1日から2020年9月30日まで)においては、期央から、新型コロナウイルス感染症の世界的な規模の感染拡大が続きました。
新型コロナウイルス感染症に対するワクチン開発等は世界的な課題となっており、感染の収束に向けて早期のワクチン開発が望まれています。当社では、2020年8月に国立研究開発法人国立がん研究センター(以下、「国立がん研究センター」)と、また同年9月に学校法人慶應義塾(以下、「慶應義塾」)と、新型コロナウイルス感染症の予防を目的としたsars-cov-2抗原パルス自家樹状細胞ワクチン(以下、「本自家樹状細胞ワクチン」)の開発に向けた共同研究開発契約を締結いたしました。本研究は国立がん研究センターが基礎データの取得、慶應義塾が非臨床試験及び第ⅰ相治験試験開始のための対応支援、当社が製造工程の構築、基礎データの取得、非臨床安全性試験等の役割を担い、本自家樹状細胞ワクチンの開発を推進してまいります。
また、当社は、新型コロナウイルス対策に貢献すべく、医療従事者の安全性を高める環境整備等の実現に資する取り組みとして、迅速、簡便に新型コロナウイルスに対する抗体を高感度に検出する新型コロナウイルス迅速抗体検査キットを当社取引先である台湾のmedigen biotechnology corporation(基亞生物科技股份有限公司、所在地:台北市、以下、「medigen社」)から仕入れ、当社取引先医療機関等に向けて2020年9月から販売を開始いたしました。
なお、当社の品川細胞培養加工施設(以下、「品川cpf」)では細胞加工体制維持のため、徹底した感染防止の取り組みを行って、感染の防止に努めてまいりました。細胞加工技術者を対象とした健康管理(検温、手洗い、消毒)の実施を、品川cpfに立ち入る全ての従業員、来客に対象を拡大しております。また、細胞加工技術者以外の職員の在宅勤務推進、社外来訪者並びに本社職員の品川cpfへの立入制限等を行うことにより、職員の感染の防止に努めております。
このような状況の中、当社は、前事業年度より引き続き、「再生医療等安全性確保法」と「医薬品医療機器等法」による法的枠組みの下、新たなビジネス展開による事業拡大に向けた取り組みを進めるとともに収益構造の改善に注力してまいりました。
当社は、2019年10月には、medigen社に対し、がんを対象疾患とするγδt(ガンマ・デルタt)細胞培養加工技術のライセンスアウトを合意し、medigen社との間でライセンス契約を締結いたしました。その後、2020年3月に共同で進めておりましたγδt(ガンマ・デルタt)細胞培養加工技術の技術移転が完了いたしました。これにより本技術を用いたがん免疫細胞治療は台湾当局の承認後、 medigen社が提携する医療機関を通じて患者様に提供されることとなります。なお、当社はライセンス契約に基づきmedigen社からロイヤリティを部分的に収受しております。
さらに2019年10月、国立がん研究センターとの間でがん抗原タンパク質の1つであるheat shock protein105 (hsp105)に関連した新たながん免疫療法の実用化に向けた共同研究契約を締結いたしました。同年11月には、京都府公立大学法人京都府立医科大学との間で、自己中和抗体産生に起因する病態を対象とした、新しいキメラ受容体(b細胞抗体受容体:barと呼びます)を遺伝子導入した免疫細胞(bar-t細胞)による特異的b細胞除去法の実用化に向けた共同研究契約を締結し、本技術に関する特許を共同出願いたしました。加えて同月には、国立大学法人九州大学との間で、慢性心不全治療に用いる再生医療等製品の実用化に向けた共同研究契約を締結いたしました。
2020年1月には、品川cpfについて「医薬品医療機器等法」に基づく「再生医療等製品製造業許可」を取得いたしました。これにより品川cpfでの再生医療等製品の製造が可能になり、再生・細胞医療の商業化に向けた製造体制のさらなる整備と取り組みを拡大させるとともに、再生医療等製品の上市実現を図ってまいります。
また、自家細胞培養軟骨「mdnt01」の開発に関しましては、前事業年度にhistogenics corporationとmedavate 社(所在地:米国コロラド州フォートコリンズ市)との間で締結された自家細胞培養軟骨「neocart®」に係る資産譲渡契約(その後、histogenics corporationはocugen社(所在地:米国ペンシルベニア州モルバーン市)と合併し、ocugen社と社名変更したため、現在の契約主体はocugen社)に基づく資産譲渡の完了に伴い、当社とhistogenics corporationとの間で締結した自家細胞培養軟骨 「neocart®」に関するライセンス契約(上記と同様の理由で現在の契約主体はocugen社)もmedavate社に承継されることから、当社は当該資産譲渡完了後、medavate社と国内における自家細胞培養軟骨「mdnt01」の開発に係る協議を進めてまいります。
当事業年度においては、新型コロナウイルス感染症の拡大による取引先医療機関でのインバウンドの患者数の減少等による細胞加工売上の減少等により、売上高は783百万円(前期比275百万円減、26.1%減)となりました。
損益面では、売上高の減少等により、売上総利益は291百万円(前期比109百万円減、27.2%減)となりましたが、事業構造改革の徹底・強化による経費の効率化等による一般管理費の減少に加えて、新型コロナウイルス感染症拡大の影響を受け、研究開発活動が一時中断、停滞したこと等による研究開発費の減少等により、販売費及び一般管理費は1,217百万円(前期比191百万円減、13.6%減)となり、営業損失は926百万円(前期は営業損失1,008百万円)となりました。
その他、投資事業組合運用益79百万円(前期比70百万円増)、貸倒引当金戻入額20百万円(前期比20百万円増)、資金調達に伴う株式交付費11百万円(前期比11百万円増)、社債発行費等8百万円(前期比0.6百万円増)等の営業外損益により、経常損失は836百万円(前期は経常損失995百万円)となりました。また、前期は特別利益231百万円及び特別損失25百万円を計上しておりましたが、当事業年度は特別利益及び特別損失の計上はなく、法人税等5百万円(前期比1百万円減)により、当期純損失は842百万円(前期は当期純損失795百万円)となりました。
報告セグメント別の業績の概況は、以下のとおりであります。
ⅰ 細胞加工業
細胞加工業については、細胞加工業の3つのビジネス領域(「特定細胞加工物製造業」・「バリューチェーン事業」・「cdmo事業」)の拡大に向けて積極的な活動を展開しております。当事業年度においては、新型コロナウイルス感染症の拡大による取引先医療機関でのインバウンドの患者数の減少等の影響による細胞加工売上の減少等により、売上高は782百万円(前期比267百万円減、25.5%減)となり、売上高の減少に伴う売上総利益の減少等により、セグメント損失は33百万円(前期はセグメント利益89百万円)となりました。
ⅱ 再生医療等製品事業
再生医療等製品事業については、再生医療等製品の早期の収益化を目指すとともに、国内外で行われている再生医療等製品の開発動向にも注目し、それらのパイプライン取得、拡充を視野に入れた活動を行っております。当事業年度においては、売上高は0.6百万円(前期比8百万円減、92.5%減)となり、新型コロナウイルス感染症拡大の影響を受け、研究開発活動が一時中断、停滞したこと等による研究開発費の減少等から、セグメント損失は392百万円(前期はセグメント損失411百万円)となりました。
(資産)
当事業年度末の総資産は、前事業年度末に比べて2,165百万円増加し、5,249百万円となりました。流動資産は3,933百万円と前事業年度末に比べ2,080百万円増加しており、主な要因は現金及び預金の増加2,240百万円、売掛金の減少118百万円、貸倒引当金の増加33百万円です。固定資産は1,316百万円と前事業年度末に比べ84百万円増加しており、主な要因は投資有価証券の増加234百万円、有形固定資産の減少99百万円、無形固定資産の減少21百万円、差入保証金の減少31百万円によるものです。
(負債)
当事業年度末の負債は、前事業年度末に比べて50百万円減少し、442百万円となりました。流動負債は273百万円で前事業年度末に比べて55百万円減少しております。主な要因は、買掛金の減少27百万円、未払金の減少24百万円です。固定負債は169百万円と前事業年度末に比べて4百万円増加しており、主な要因は、繰延税金負債の増加8百万円、リース債務の減少4百万円です。
(純資産)
当事業年度末の純資産は、前事業年度末に比べて2,216百万円増加し、4,806百万円となりました。主な要因は、新株予約権の行使による資本金1,410百万円及び資本剰余金1,410百万円の増加、その他有価証券評価差額金232百万円の増加の一方、当期純損失842百万円の減少によるものです。
この結果、自己資本比率は、前事業年度末の82.7%から90.7%となりました。
②キャッシュ・フローの状況
当事業年度末における現金及び現金同等物(以下「資金」という。)は、前事業年度末に比べ2,240百万円増加し、当事業年度末には3,643百万円となりました。
当事業年度における各キャッシュ・フローの状況とそれらの要因は、次のとおりであります。
(営業活動によるキャッシュ・フロー)
営業活動に使用した資金は632百万円(前期は938百万円の使用)となりました。
主な増加は、減価償却費154百万円、売上債権の減少額118百万円であり、主な減少は、税引前当期純損失836百万円、投資事業組合運用益79百万円です。
(投資活動によるキャッシュ・フロー)
投資活動によって獲得した資金は86百万円(前期は50百万円の獲得)となりました。
主な収入は、投資事業組合からの分配による収入85百万円、長期貸付金の回収による収入20百万円であり、主な支出は、資産除去債務の履行による支出31百万円です。
(財務活動によるキャッシュ・フロー)
財務活動によって獲得した資金は2,786百万円(前期は90百万円の獲得)となりました。
収入は、株式の発行による収入2,765百万円、新株予約権の発行による収入41百万円であり、支出は、リース債務の返済による支出20百万円です。
決算(直近四半期)
2【経営者による財政状態、経営成績及びキャッシュ・フローの状況の分析】
(1)経営成績の状況
当第3四半期累計期間(2019年10月1日から2020年6月30日まで)において当社は、前事業年度より引き続き、「再生医療等の安全性の確保等に関する法律」と「医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律」による法的枠組みの下、新たなビジネス展開による事業拡大に向けた取り組みを進めるとともに収益構造の改善に注力しております。
当社は、2019年10月には、台北証券取引所上場企業であるmedigen biotechnology corporation(基亞生物科技股份有限公司、所在地:台北市、以下、「mbc」)に対し、がんを対象疾患とするγδt(ガンマ・デルタt)細胞培養加工技術のライセンスアウトを合意し、ライセンス契約を締結いたしました。その後、2020年3月に共同で進めておりましたγδt(ガンマ・デルタt)細胞培養加工技術の技術移転が完了いたしました。これにより本技術を用いたがん免疫細胞治療は台湾当局の承認後、mbcが提携する医療機関を通じて患者様に提供されることとなり、当社はmbcからγδt(ガンマ・デルタt)細胞培養加工技術を用いた培養加工件数に応じたロイヤリティを収受することとなります。
さらに2019年10月、国立研究開発法人国立がん研究センターとの間でがん抗原タンパク質の1つであるheat shock protein105 (hsp105)に関連した新たながん免疫療法の実用化に向けた共同研究契約を締結いたしました。同年11月には、京都府公立大学法人京都府立医科大学との間で、自己中和抗体産生に起因する病態を対象とした、新しいキメラ受容体(b細胞抗体受容体:barと呼びます)を遺伝子導入した免疫細胞(bar-t細胞)による特異的b細胞除去法の実用化に向けた共同研究契約を締結し、本技術に関する特許を共同出願いたしました。加えて同月には、国立大学法人九州大学との間で、慢性心不全治療に用いる再生医療等製品の実用化に向けた共同研究契約を締結いたしました。
2020年1月には、品川細胞培養加工施設(以下、「品川cpf」)について「医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律」に基づく「再生医療等製品製造業許可」を取得しました。これにより品川cpfでの再生医療等製品の製造が可能になり、再生・細胞医療の商業化に向けた製造体制のさらなる整備と取り組みを拡大させるとともに、再生医療等製品の上市実現を図ってまいります。
また、自家細胞培養軟骨「mdnt01」の開発に関しましては、前事業年度にhistogenics corporationとmedavate 社(所在地:米国コロラド州フォートコリンズ市)との間で締結された自家細胞培養軟骨「neocart®」に係る資産譲渡契約に基づく資産譲渡の完了に伴い、当社とhistogenics corporationとの間で締結した自家細胞培養軟骨 「neocart®」に関するライセンス契約もmedavate社に承継されることから、当社は当該資産譲渡完了後、medavate社と国内における自家細胞培養軟骨「mdnt01」の開発に係る協議を進めてまいります。
このように新たな取り組みを進めるとともに、製造体制の効率化による生産性の向上と新規顧客の獲得などにより収益の拡大に努めております。
一方、新型コロナウイルス感染症の拡大と長期化による影響は、経済活動の停滞や個人消費の低迷等広範囲に表れておりますが、その影響は当社及び当社の契約医療機関にも及んでおり、当社を取り巻く事業環境は、先行きが不透明な状況にあります。
このような状況下において、当社の品川cpfでは細胞加工体制維持のため、徹底した感染防止の取り組みを行っており、細胞加工技術者を対象とした健康管理(検温、手洗い、消毒)の実施を、品川cpfに立ち入る全ての従業員、来客に対象を拡大しております。また、細胞加工技術者以外の職員の在宅勤務推進、社外来訪者並びに本社職員の品川cpfへの立入制限等を行うことにより、職員の感染の防止に努めております。
これらの結果、当第3四半期累計期間における当社の経営成績は以下のとおりとなりました。
(金額単位:百万円)
| 売上高 | 営業損失(△) | 経常損失(△) | 四半期純損失(△) | 1株当たり 四半期純損失 (△) |
当第3四半期 累計期間 | 637 | △642 | △629 | △633 | △4.90円 |
前第3四半期 累計期間 | 755 | △855 | △887 | △807 | △6.83円 |
増減率(%) | △15.6 | - | - | - | - |
当第3四半期累計期間においては、新型コロナウイルス感染症の拡大による取引先医療機関でのインバウンドの患者数の減少等による細胞加工売上の減少等により、売上高は637百万円(前年同期比15.6%減)となりました。損益面につきましては、売上高の減少等により、売上総利益は249百万円(前年同期比3.7%減)となりましたが、事業構造改革の徹底・強化による販売管理費の効率化等による販売費、一般管理費の減少に加えて、新型コロナウイルス感染症拡大の影響を受け、研究開発活動が一時中断、停滞したこと等による研究開発費の減少等により、販売費及び一般管理費は892百万円(前年同期比19.9%減)となり、営業損失は642百万円(前年同期は営業損失855百万円)となりました。また、第2四半期累計期間において貸倒引当金戻入額12百万円を計上しておりましたが、当第3四半期会計期間において、貸倒引当金を計上している長期貸付金の一部を回収したことにより貸倒引当金戻入額6百万円を計上したことから、貸倒引当金戻入額18百万円を営業外収益に計上いたしました。さらに、資金調達に伴う株式交付費5百万円、社債発行費等4百万円を営業外費用に計上したこと等により、経常損失は629百万円(前年同期は経常損失887百万円)、四半期純損失は633百万円(前年同期は四半期純損失807百万円)となりました。
報告セグメント別の経営成績の概況は、以下のとおりであります。
(金額単位:百万円)
| 報告セグメント | 調整額 (注)1 | 四半期損益計算書 計上額(注)2 | ||||
細胞加工業 | 再生医療等製品事業 | ||||||
売上高 | セグメント 利益 | 売上高 | セグメント 損失(△) | セグメント 損失(△) | 売上高 | セグメント 損失(△) | |
当第3四半期 累計期間 | 636 | 28 | 0 | △291 | △380 | 637 | △642 |
前第3四半期 累計期間 | 752 | 16 | 2 | △333 | △537 | 755 | △855 |
(注)1.セグメント損失(△)の調整額は、全社費用であります。全社費用は、報告セグメントに帰属しない一般管理費であります。
2.セグメント損失(△)は、四半期損益計算書の営業損失と調整を行っています。
① 細胞加工業
細胞加工業については、細胞加工業の3つのビジネス領域(「特定細胞加工物製造業」・「バリューチェーン事業」・「cdmo事業」)の拡大に向けて積極的な活動を展開しております。当第3四半期累計期間においては、新型コロナウイルス感染症の拡大による取引先医療機関でのインバウンドの患者数の減少等の影響による細胞加工売上の減少等により、売上高は636百万円(前年同期比15.4%減)となり、事業構造改革の徹底・強化による販売管理費の効率化等により、セグメント利益は28百万円(前年同期比73.9%増)となりました。
② 再生医療等製品事業
再生医療等製品事業については、再生医療等製品の早期の収益化を目指すとともに、国内外で行われている再生医療等製品の開発動向にも注目し、それらのパイプライン取得、拡充を視野に入れた活動を行っております。当第3四半期累計期間においては、売上高は0百万円(前年同期比76.6%減)となり、新型コロナウイルス感染症拡大の影響を受け、研究開発活動が一時中断、停滞したこと等による研究開発費の減少等により、セグメント損失は291百万円(前年同期はセグメント損失333百万円)となりました。
(2)財政状態の状況
(財政状態)
| 前事業年度末 | 当第3四半期 会計期間末 | 増減 |
資産合計(百万円) | 3,084 | 3,846 | 762 |
負債合計(百万円) | 493 | 396 | △97 |
純資産合計(百万円) | 2,590 | 3,450 | 859 |
自己資本比率(%) | 82.7 | 89.1 | 6.4 |
1株当たり純資産(円) | 21.10 | 24.07 | 2.97 |
資産合計は、現金及び預金772百万円増加、投資有価証券286百万円増加、売掛金138百万円減少、建物(純額)80百万円減少等により、前事業年度末に比べて762百万円増加しました。
負債合計は、前事業年度末に比べて97百万円減少しました。主な減少は、買掛金26百万円、賞与引当金26百万円、未払法人税等14百万円です。
純資産合計は、四半期純損失633百万円による減少の一方、新株予約権の行使による資本金572百万円、資本剰余金572百万円及びその他有価証券評価差額金363百万円の増加等により、前事業年度末に比べて859百万円増加しました。
以上の結果、自己資本比率は、前事業年度末の82.7%から89.1%となりました。
(3)経営方針・経営戦略等
当第3四半期累計期間において、当社が定めている経営方針・経営戦略等について重要な変更はありません。
(4)事業上及び財務上の対処すべき課題
当第3四半期累計期間において、当社の事業上及び財務上の対処すべき課題に重要な変更及び新たに生じた課題はありません。
(5)研究開発活動
当第3四半期累計期間における研究開発活動の金額は、188百万円であります。
① 細胞加工業
当第3四半期累計期間において、細胞加工業に係る研究開発活動の状況に重要な変更はありません。
なお、当第3四半期累計期間における細胞加工業に係る研究開発費は20百万円であります。
② 再生医療等製品事業
当第3四半期累計期間における再生医療等製品事業に係る研究開発費は167百万円であります。
第1四半期会計期間においては、「mdnt01」や「atl-dc-101」に続く、開発シーズとして、国立大学法人九州大学と慢性心不全治療に用いる再生医療等製品の実用化に向けた共同研究契約を締結いたしました。当社がこれまでがんの免疫細胞加工技術で培ったノウハウをがん以外の疾患へ応用し、慢性心不全治療のための再生医療等製品の開発に取り組む予定です。さらに国立研究開発法人国立がん研究センターとhsp由来ペプチドに関する研究成果をもとにした新規のがん免疫療法の実用化に向けた共同研究及び京都府公立大学法人京都府立医科大学と自己中和抗体産生に起因する病態を対象とした新しいキメラ受容体(b細胞抗体受容体)を遺伝子導入した免疫細胞による特異的b細胞除去法の実用化に向けた共同研究を開始いたしました。
第2四半期会計期間においては、当社は、2018年3月に独立行政法人国立病院機構(以下「国立病院機構」)との間で「成人t細胞白血病を対象とした樹状細胞ワクチン」(以下「atl-dc-101」)の再生医療等製品としての製造販売承認取得を目的とした共同開発契約を締結し、2019年9月期第4四半期中の第ⅱ相医師主導治験の治験届の提出を目指し共同開発を推進してまいりましたが、製造面等の様々な要因により開発遅延が生じ、両者で今後の開発計画等を総合的に勘案した結果、当社における製品開発の優先順位を見直さざるを得なくなったため、2020年1月、当該共同開発を中止し、共同開発契約を合意解約することを発表いたしました。
(6)事業等のリスクに記載した重要事象等を改善するための対応策
当社は、前記「1 事業等のリスク」に記載のとおり、継続企業の前提に疑義を生じさせるリスクが存在しております。
しかしながら、当社は、2018年4月に開始した事業構造改革を着実に実行することで、細胞加工業セグメントにおいては細胞加工施設の統廃合、希望退職募集の実施等を通じて製造体制の適正化を図り、前事業年度に引き続き第3四半期累計期間において同セグメントのセグメント利益の黒字化を達成いたしました。一方、再生医療等製品事業セグメントにおいては、早期の製造販売承認の取得に向けて有望でかつ可能性の高いシーズを優先して開発を進めるとともに、再生医療等製品の開発費等については資金状況を勘案の上、機動的に資金調達を実施してまいります。現状では、構造改革の着実な実行を通じた資金の確保、さらに2019年6月の第14回及び第15回並びに2020年7月の第16回の新株予約権の発行による再生医療等製品開発費の資金調達等により、安定的なキャッシュポジションを維持しており、当面の資金繰りに懸念はないものと判断しております。これらに加えて、当社における当第3四半期会計期間末の資金残高の状況を総合的に検討した結果、事業活動の継続性に疑念はなく、継続企業の前提に関する重要な不確実性は認められないものと判断しております。
経営方針
当社は、常に本質を究め、誠実性と公正性をもって真の社会的付加価値を創造するという経営理念の下、次世代の医療を支える革新的な技術及びサービスを迅速かつ効率的に社会に提供することにより、人々の健康と“quality of life(生活の質)”の向上に資することを使命として事業を展開しており、独自の研究開発、技術開発はもとより、国内外の医療機関や研究機関、企業その他との広範で柔軟なコラボレーションを積極的に推進することにより、事業の成長スピードを早め、より大きな事業機会の創出を図ることを経営の基本方針とします。
戦略
2014年11月に再生・細胞医療を、より安全により早く患者に届けることができる、新たな2つの法的枠組みが設けられました。1つは「再生医療等の安全性の確保等に関する法律」(以下、「再生医療等安全性確保法」)で、これまでは医療機関のみが許されていた治療に用いる細胞加工について、特定細胞加工物製造許可を取得した企業が細胞加工を受託できるようになりました。もう1つは「医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律」(以下、「医薬品医療機器等法」)で、従来の医薬品、医療機器とは別に「再生医療等製品」という新たなカテゴリーが設けられ、安全性が確保され効果が推定されれば、条件・期限付きで早期に承認される仕組みが導入されました。これらの新たな法的枠組みの下、当社は、新たなビジネス展開による事業拡大に向けた取り組みを進めております。
当社は、1999年から免疫細胞治療に用いる細胞の加工のほか、免疫細胞治療を実施する際に必要となる細胞培養加工施設の設置・運営管理を始め、細胞加工技術者、信頼性保証、技術開発などを医療機関に対して提供してまいりました。これまで経験してきた細胞加工件数は18万件以上に及びます。また、国家戦略特区に位置する羽田空港近隣に、日米欧の規制対応を踏まえた最新鋭の細胞培養加工施設(以下、「品川cpf」)を保有しております。品川cpfは、2015年5月に特定細胞加工製造許可を取得し、続いて2020年1月には再生医療等製品製造業許可を取得したことにより、特定細胞加工物の開発・製造受託と再生医療等製品の開発から商業生産まで、様々な細胞や組織の加工を行うことが可能な施設となっております。当社は、これらを当社の競合他社に対する競争優位性と考えております。
現在はこれらの当社の強みを生かすことができる主力事業の特定細胞加工物の製造受託において、主に医療機関等から免疫細胞治療に用いる細胞の加工を受託しております。今後はさらに、体細胞や体性幹細胞を用いた細胞などの加工を受託するとともに、バリューチェーン事業において、研究から開発、製造、マーケティングといった再生・細胞医療のバリューチェーンをワンストップで実現するトータルソリューションを提供することで、お客様がスムーズに再生・細胞医療を実施できるよう、様々な支援を行ってまいります。これらに加えて、cdmo事業において、企業から再生医療等製品や治験製品の開発・製造受託を図ってまいります。
当社を取り巻く環境につきましては、新型コロナウイルス感染症の感染の拡大が、未だに収束の見通しが立っておらず、引き続き企業活動や経済活動への制限を余儀なくされるような厳しい状況が続くものと想定されます。
このような状況下、当社は、新型コロナウイルス感染症の対策として、品川cpfの従業員及び来訪者の健康管理(検温、手洗い、消毒)の実施や本社等の職員の在宅勤務推進など徹底した感染の防止に努めております。
課題
「(3)中長期的な会社の経営戦略」を踏まえ、当社が対処すべき特に重要な課題は、以下のとおりであります。
① 細胞加工業の推進
当社がこれまで18万件以上の細胞加工実績で培ってきたノウハウ・経験をもとに、再生・細胞医療に取り組む製薬企業、大学、医療機関/研究機関等から、特定細胞加工物や再生医療等製品/治験製品の製造を受託する「細胞加工業」や「cdmo事業」の売上を拡大してまいります。また、これから需要拡大が見込まれる再生・細胞医療のコンサルティング、細胞培養加工施設の運営管理、細胞加工技術者の派遣・教育システムの提供等といった「バリューチェーン事業」の売上拡大にも注力してまいります。
② 再生医療等製品の開発
当社が行っている免疫細胞治療に係る研究開発に加えて、国内外において有望な再生医療等製品シーズを保有する企業等とのアライアンスにより、開発パイプラインを拡充し、再生医療等製品の開発を加速してまいります。同時に、再生医療等製品の製造販売承認を取得することにより、売上の拡大を図ってまいります。
沿革
2【沿革】
年月 | 事項 |
1995年10月 | 予防医学に基づく新たな医療サービスの提供を目的として、東京都港区に株式会社メディネット(資本金1,000万円)を設立 |
1999年4月 | 東京都世田谷区に分子免疫学研究所を開設、契約医療機関向けに細胞培養加工施設を設置し、免疫細胞療法総合支援サービスを開始 |
2000年12月 | 東京都港区に本社を移転 |
2001年8月 | 厚生労働省による新事業創出促進法に基づく「新事業分野開拓の実施に関する計画」の認定 |
10月 | 神奈川県横浜市港北区に本社を移転、契約医療機関向けに細胞培養加工施設(新横浜cpc1)を設置し、免疫細胞療法総合支援サービスを開始 |
2002年4月 | 神奈川県横浜市港北区に先端医学研究所を開設 |
7月 | 契約医療機関向けに細胞培養加工施設(新横浜cpc2)を増設 |
2003年5月
| 東京都世田谷区に研究開発センターを新設、分子免疫学研究所と先端医学研究所を同センター内に移転すると共に、先端医学研究所を「分子遺伝学研究所」に改称 |
6月 | 大阪府吹田市に大阪事業所を開設、契約医療機関向けに細胞培養加工施設(大阪cpc)を設置し、免疫細胞療法総合支援サービスを開始 |
10月 | 福岡県福岡市博多区に福岡事業所を開設、契約医療機関向けに細胞培養加工施設(福岡cpc)を設置し、免疫細胞療法総合支援サービスを開始 |
| 東京証券取引所マザーズ市場へ株式を上場(2003年10月8日付) |
2004年3月 | 細胞医療支援事業においてiso9001の認証を取得 |
5月 | 「分子免疫学研究所」と「分子遺伝学研究所」を統合し、研究開発センターの名称を「先端医科学研究所」に改称 |
8月 | 日本初の治療用がん組織保管サービスである「自己がん組織バンク」サービスを開始 |
2007年2月
| 東京大学医学部附属病院の22世紀医療センター内に開設された「免疫細胞治療学講座(免疫細胞治療部門)」向けに細胞培養加工施設(東大22世紀医療センターcpc)を設置し、免疫細胞療法総合支援サービスを開始 |
6月 | 独立行政法人国立病院機構大阪医療センターと同センターにおける免疫細胞療法の実施に対する技術支援を行うライセンス契約を締結 |
11月 | 研究開発施設を東京都世田谷区の先端医科学研究所に統合し、名称を「研究開発センター」に改称 |
2008年1月 | 100%子会社として株式会社医業経営研究所を設立 |
2011年7月 | 九州大学先端医療イノベーションセンター向けに免疫細胞療法総合支援サービスを開始 |
2013年12月 | 100%子会社として株式会社メドセルを設立 |
2015年5月 | 細胞加工事業の拡大を目指して、東京都品川区に再生・細胞医療用の細胞培養加工施設(品川cpf)を建設し、特定細胞加工物製造許可を取得 |
2016年6月 | 研究開発部門(研究開発センター)を本社に移転 |
2017年8月 | 福岡細胞培養加工施設(福岡cpc)を新横浜細胞培養加工施設(新横浜cpc)に統合 |
10月 | 新横浜細胞培養加工施設(新横浜cpc)及び大阪細胞培養加工施設(大阪cpc)の特定細胞加工物製造許可を取得 |
2018年8月 | 大阪細胞培養加工施設(大阪cpc)を新横浜細胞培養加工施設(新横浜cpc)に統合 |
| 100%子会社であった株式会社医業経営研究所及び株式会社メドセルと吸収合併契約を締結(2018年10月1日合併効力発生) |
2019年4月 | 新横浜細胞培養加工施設(新横浜cpc)を品川細胞培養加工施設(品川cpf)に統合 |
6月 | 本社を東京都大田区に移転 |
2020年1月 | 品川細胞培養加工施設(品川cpf)の再生医療等製品製造業許可を取得 |
配当政策
3【配当政策】
当社では、株主に対する利益還元を最重要課題の一つとして位置づけており、業績、経営基盤の強化及び将来の成長等を総合的に勘案して、利益配当の実施を検討してまいります。また、先行投資を着実に回収し、継続的な成長を果たすことで企業価値を向上し、株主の皆様の利益に貢献したいと考えております。
しかしながら当社は、これまで、配当を実施した実績はなく、当期末では累積損失が発生しています。そのため先ずは内部留保を確保して、早期の累積損失の解消に努めるとともに、再生医療等製品の製造・販売承認の取得に向けた設備投資及び研究開発投資、細胞加工業の顧客獲得に向けた設備投資及び営業活動への資金充当を優先させ、企業体質の強化を進めるとともに、事業の成長を図っていく方針であります。
当社は、中間配当と期末配当の年2回の剰余金の配当を行うことを基本方針としており、これらの剰余金の配当の決定機関は、期末配当については株主総会、中間配当については取締役会であります。
なお、当社は、「取締役会の決議により、毎年3月31日を基準日として、中間配当を行うことができる」旨を定款に定めております。
株式の状況
②【発行済株式】
種類 | 事業年度末現在発行数(株) (2020年9月30日) | 提出日現在発行数(株) (2020年12月17日) | 上場金融商品取引所名又は登録認可金融商品取引業協会名 | 内容 |
普通株式 | 160,830,423 | 165,860,423 | 東京証券取引所 (マザーズ) | 権利内容に何ら限定のない当社における標準となる株式であり、単元株式数は100株であります。 |
計 | 160,830,423 | 165,860,423 | - | - |
(注)「提出日現在発行数」欄には、2020年12月1日からこの有価証券報告書提出日までの新株予約権の行使により発行された株式数は含まれておりません。
(5)【所有者別状況】
|
|
|
|
|
|
| 2020年9月30日現在 | ||
区分 | 株式の状況(1単元の株式数100株) | 単元未満株式の状況 (株) | |||||||
政府及び地方公共団体 | 金融機関 | 金融商品取引業者 | その他の法人 | 外国法人等 | 個人その他 | 計 | |||
個人以外 | 個人 | ||||||||
株主数(人) | - | 1 | 37 | 189 | 31 | 95 | 55,198 | 55,551 | - |
所有株式数(単元) | - | 23,290 | 62,597 | 50,490 | 53,381 | 1,660 | 1,416,733 | 1,608,151 | 15,323 |
所有株式数の割合(%) | - | 1.44 | 3.89 | 3.13 | 3.31 | 0.10 | 88.09 | 100.00 | - |
(注)上記「その他の法人」の欄には、証券保管振替機構名義の株式が24単元含まれております。
(6)【大株主の状況】
|
| 2020年9月30日現在 | |
氏名又は名称 | 住所 | 所有株式数(株) | 発行済株式(自己株式を除く。)の総数に対する所有株式数の割合(%) |
木村佳司 | 千葉県浦安市 | 7,629,300 | 4.74 |
macquarie bank limited dbu ac (常任代理人 シティバンク、エヌ・エイ東京支店) | level3,1 martin place sydney nsw 2000 australia (東京都新宿区新宿6-27-30) | 3,583,200 | 2.22 |
日本証券金融株式会社 | 東京都中央区日本橋茅場町1-2-10 | 2,329,000 | 1.44 |
株式会社sbi証券 | 東京都港区六本木1-6-1 | 1,416,203 | 0.88 |
ihn株式会社 | 千葉県浦安市入船3-68-5 | 1,400,000 | 0.87 |
森部鐘弘 | 愛知県名古屋市東区 | 1,110,000 | 0.69 |
中埜昌美 | 愛知県半田市 | 1,000,000 | 0.62 |
楽天証券株式会社 | 東京都港区南青山2-6-21 | 740,500 | 0.46 |
smbc日興証券株式会社 | 東京都千代田区丸の内3-3-1 | 688,500 | 0.42 |
王丹 | 千葉県千葉市中央区 | 510,000 | 0.31 |
計 | - | 20,406,703 | 12.68 |
(注)2020年10月6日付で公衆の縦覧に供されている変更報告書において、マッコーリー バンク リミテッド(macquarie bank limited)が2020年9月30日現在で以下のとおり株式を保有している旨の記載がありますが、当社として2020年9月30日現在における実質所有株式数の確認ができませんので、上記大株主の状況には含めておりません。
氏名又は名称 | 住所 | 保有株券等の数 (株) | 株券等保有割合 (%) |
マッコーリー バンク リミテッド (macquarie bank limited) | オーストラリア連邦ニューサウスウェールズ州2000 シドニー マーティンプレイス 50 レベル6 | 株式 2,946,100 新株予約権 16,900,000 | 11.17 |
(注)上記「株券等保有割合」には、新株予約権の保有に伴う潜在株式の数が16,900,000株含まれております。
役員の状況
男性10名 女性-名 (役員のうち女性の比率-%)
役職名 | 氏名 | 生年月日 | 略歴 | 任期 | 所有株式数 (株) | ||||||||||||||||||||||||||||||||
代表取締役 社長 | 木村 佳司 | 1952年3月15日生 |
| (注)3 | 7,629,300 | ||||||||||||||||||||||||||||||||
取締役 経営管理部長 | 落合 雅三 | 1974年9月22日生 |
| (注)3 | 33,300 | ||||||||||||||||||||||||||||||||
取締役 細胞加工事業部長 | 近藤 隆重 | 1975年4月22日生 |
| (注)3 | 28,100 | ||||||||||||||||||||||||||||||||
取締役 | 久布白 兼直 | 1960年7月17日生 |
| (注)3 | - |
役職名 | 氏名 | 生年月日 | 略歴 | 任期 | 所有株式数 (株) | ||||||||||||||||||||||||||||||||||
取締役 | 木村 友則 | 1982年11月10日生 |
| (注)3 | - | ||||||||||||||||||||||||||||||||||
取締役 | 篠田 丈 | 1961年8月1日生 |
| (注)3 | 80,500 | ||||||||||||||||||||||||||||||||||
取締役 | 吉野 公一郎 | 1949年3月25日生 |
| (注)3 | 100,000 |
役職名 | 氏名 | 生年月日 | 略歴 | 任期 | 所有株式数 (株) | ||||||||||||||||||||||||||
常勤監査役 | 瀧上 眞次 | 1952年9月17日生 |
| (注)4 | 3,000 | ||||||||||||||||||||||||||
監査役 | 片山 卓朗 | 1950年10月8日生 |
| (注)4 | - | ||||||||||||||||||||||||||
監査役 | 長谷川 明彦 | 1951年7月27日生 |
| (注)5 | - | ||||||||||||||||||||||||||
計 | 7,874,200 | ||||||||||||||||||||||||||||||
(注)1.取締役篠田丈氏及び吉野公一郎氏は、社外取締役であります。
2.監査役瀧上眞次氏、片山卓朗氏及び長谷川明彦氏は、社外監査役であります。
3.2020年12月17日開催の定時株主総会の終結の時から2年間であります。
4.2018年12月20日開催の定時株主総会の終結の時から4年間であります。
5.2020年12月17日開催の定時株主総会の終結の時から4年間であります。
6.所有株式数には、役員持株会名義のものは含めておりません。
7.代表取締役社長木村佳司氏と取締役木村友則氏は、親子であります。